<
section style="white-space: normal; background-color: rgb(255, 255, 255);">
近日,上海有机所张国柱研究员课题组在Angew发表论文,报道了通过铜催化,实现炔烃和α-溴代酰胺之间的不对称Sonogashira偶联反应。该方法使用两种简单易得的起始原料,以高对映选择性的方式合成了具有重要应用价值的β,γ-炔基酰胺衍生物。同时,双噁唑啉二苯基苯胺(BOPA,L4)可作为有效的手性配体。此外,该反应机理涉及烷基自由基的形成。文章链接DOI:10.1002/anie.202000860
跳转阅读→化工医药企业HR注意啦,这里有近千位化学化工医药专业的海内外本硕博毕业生等你招聘~
(图片来源:Angew. Chem. Int. Ed.)
在过渡金属催化下,通过不对称配体的调控,实现烷基亲电试剂与预官能化亲核试剂(如有机锌、有机硼、格氏试剂和有机硅烷试剂)之间的交叉偶联反应,是合成高对映体产物的高效方法之一。在此类反应中,通过α-卤代羰基及其衍生物(如腈、磺酸盐、磷酸盐、酰胺等)的偶联反应,可获得具有价值的α-官能团化的羰基化合物。尽管对于羰基化合物中α-官能团化的C(sp3)和C(sp2)偶联反应已被大量研究,但对羰基化合物的C(sp)报道却很少,可能是由于炔烃上易发生副反应。此外,内炔烃一直是天然产物、生物活性分子、功能材料中重要的结构单元,因此,将C≡C引入体系中一直是研究的热点。早在2003年,G. F. Fu课题组将催化量的钯盐、铜盐与N-杂环卡宾配体结合,实现了末端炔烃与未活化伯溴(碘)化物的偶联反应。受此启发,其他课题组也开始探索其它金属/配体的催化体系,以实现仲烷基卤化物和α-羰基卤化物的偶联反应。如雷爱文课题组,通过Pd-催化Stille和Suzuki反应,实现了金属炔化物(炔基锡烷和炔基三氟硼酸盐)与α-卤代羰基化合物的偶联反应(Scheme 1, eq. 1)。Oshima课题组,通过串联自由基加成-断裂过程,实现了镓或铟的炔化物与α-卤代羰基化合物的反应。G. F. Fu课题组,使用Cu-催化经卡宾中间体,实现了炔烃和重氮羰基化合物反应。Nishikata课题组,开发了一种Cu-催化α-溴酰胺的Sonogashira偶联反应,合成了含有季碳中心的衍生物,其中炔化铜是关键的中间体。近期,李朝军课题组通过光催化,实现了末端炔烃和α-羰基卤化物的偶联反应(eq. 2)。尽管已取得一定的进展,但据文献查阅,关于末端炔烃与α-羰基卤化物的不对称Sonogashira偶联反应却很少。刘心元课题组报道了在铜催化下,使用手性金鸡纳生物碱衍生的P,N-配体,实现了末端炔烃和外消旋烷基卤化物之间C(sp3)-C(sp)的Sonogashira交叉偶联反应,并且以α-溴酰胺作为底物,具有良好的收率和ee值(eq. 3)。鉴于α-炔基羰基化合物的重要性,仍需一种可从市售化合物(如炔烃和α-卤代羰基化合物)直接合成具有高对映选择性的α-炔基羰基化合物的手性催化体系。在此,上海有机所张国柱研究员课题组报道了铜催化的不对称Sonogashira交叉偶联反应,使用市售的α-卤代酰胺与未官能化的末端炔烃作为底物,合成了多种β,γ-炔基酰胺衍生物(eq. 4)。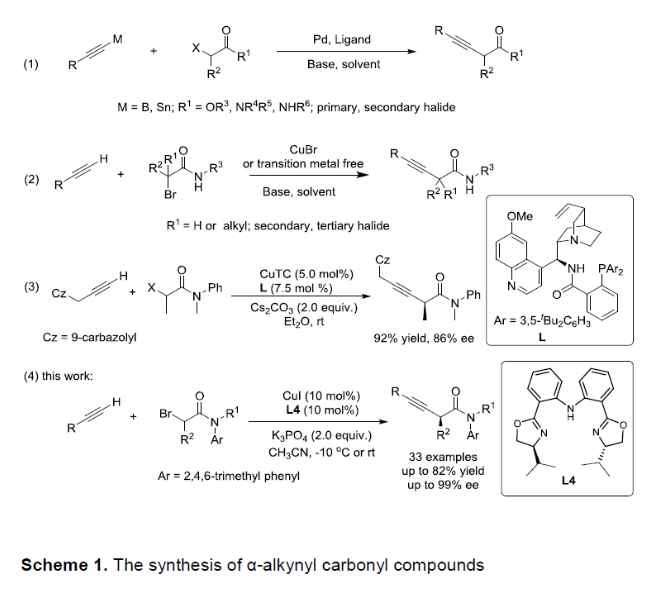
(图片来源:Angew. Chem. Int. Ed.)<br/>
首先,作者以市售的N-苄基-2-溴-N-苯基丙酰胺b1与苯乙炔a作为模型底物,对反应条件进行了筛选(Table 1)。当使用不同取代基的Cbzbox配体(L1-L3)时,可获得相应的产物c1,但ee值很低(entries 1-3)。令作者惊讶的是,当使用CuI作为催化剂,iPr-BOPA (L4)作为配体,K3PO4作为碱时,可以80%的产率获得目标产物c1,ee值为76%(entry 4)。而使用L5时,表现出较低的对映选择性,L6-L8对于当前反应无效。若将反应温度降低至-10 ℃时,可将ee值进一步提高至90%,收率不受影响(entry 9)。此外,作者发现,R2的取代基对于提高反应的效率至关重要。当使用含有1,3,5-三甲基苯取代b2底物时,在-10 ℃下与苯乙炔反应生成c2,产率为84%,ee为94%(entry 11)。而使用b3和b4底物时,反应效率有所下降,使用b5底物时则不反应(entries 12-14)。
(图片来源:Angew. Chem. Int. Ed.)
在获得上述最佳反应条件后,作者对α-溴代酰胺与各种炔烃底物范围进行了考察(Table 2)。首先,作者选择了一些芳基取代的炔烃,反应均具有良好的兼容性,含有N,N-二甲基、甲氧基、烷基、卤素等取代的芳基炔烃,均可顺利反应,获得相应的产物c5-c13。除芳族炔烃外,烷基和环烷基取代的炔烃,也可获得目标产物c14-c17。同时,甲硅烷基取代的炔烃,均以良好的收率和优异的对映选择性获得相应的产物c18-c19。值得注意的是,含有羰基和四个连续的手性中心的3-乙炔基雌酮化合物,通过此方法进行修饰后,获得产物c20,产率为70%,dr > 20:1。
(图片来源:Angew. Chem. Int. Ed.)
此外,根据反应条件的筛选,作者发现,含有2,4,6-三甲基苯基的α-溴代酰胺底物对于立体选择性的控制至关重要。因此,作者将其固定,并对酰胺上的氮取代基R2进行了考察,含有富电子或缺电子的苄基(烷基)均可获得相应的产物c21-c28。同时,含有噻吩和萘取代基的底物也可得到相应的产物c29和c30。随后,作者对α-碳上的取代基R1范围进行了扩展。当α-烷基改为Et或nBu时,可获得产物c31和c32,收率为72%-75%,ee值高达99%。但是,当前的催化体系不能与其它α-溴羰基化合物反应,如ɑ-溴代酸酯、α-溴腈等,均生成烯烃副产物。 (图片来源:Angew. Chem. Int. Ed.)为了进一步了解反应机理,作者进行了一些对照实验(Scheme 2)。首先,通过CuX和苯乙炔制备乙炔铜中间体A1。在没有BOPA配体或碱时,A1不会与b2反应,表明这配体和碱对于偶联反应至关重要(eq. 5)。当使用配体(1.0 eq)和K3PO4(1.0 eq)时,获得67%收率的产物c2(ee为95%)。该结果表明A1可能是该反应关键的中间体。同时,作者还向反应体系中加入了TEMPO,仅需10 mol%即可终止反应(eq. 6)。b18与苯乙炔反应获得少量顺式环化产物d1(eq. 7),作为仲烷基自由基环化反应的典型代表(反应性和选择性)。这些结果暗示在该反应中可能产生自由基。与假设一致,当以(S,S)-L4或(R,R)-L4作为手性配体时,会获得相反对映体的产物,从而说明配体的构型决定产物的构型(eq. 8)。此外,(+)-b2与炔烃反应良好,但残留的溴化物的对映体纯度显著降低,表明烷基溴化物可快速消旋化(eq. 9)。
(图片来源:Angew. Chem. Int. Ed.)
根据上述实验和相关文献的查阅,作者提出了一种可能的反应机理(Figure 1)。在碱性条件下,Cu(I)X与L进行配体交换,生成配合物Cu(I)L。随后,与RC≡CH配位形成[LCu(I)(C≡CR)]-K+中间体A。紧接着,α-溴酰胺经还原获得铜(II)配合物LCu(II)(C≡CR)和烷基自由基B。最后,经历两种可能的途径,在path a中,烷基自由基与铜(II) 配合物经氧化加成,生成铜(III)配合物C,再经还原消除,生成目标产物,并再生催化剂。而在path b中,烷基自由基可直接与铜(II)配合物发生配位,从而获得相同的结果。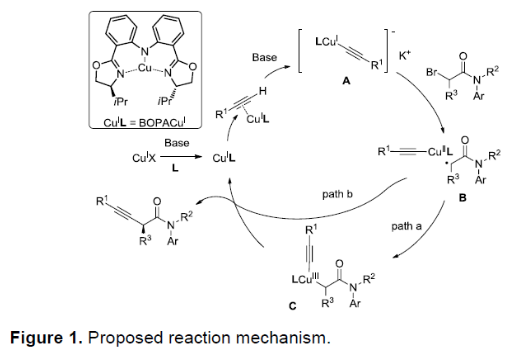
(图片来源:Angew. Chem. Int. Ed.)
β,γ-炔基酰胺衍生物作为合成复杂分子通用的中间体,通过对其后期修饰则可进一步证明该反应的实用性(Scheme 3)。如使用催化剂H2SiF6,可将TMS保护基去除,获得末端炔烃产物e1,同时保持了对映体纯度(eq. 10)。然而,用催化性TBD与c2反应时,获得桥连多环内酰胺f1(外消旋形式)(eq. 11)。此外,通过酸性水合作用,可以容易地获得1,4-二酮化合物g1(eq. 12)。
(图片来源:Angew. Chem. Int. Ed.)
总结:上海有机所张国柱研究员课题组报道了一种高效且通用的铜催化α-溴代酰胺与炔烃的不对称Sonogashira偶联反应,具有反应条件温和、原料廉价易得、底物范围广泛等优点。同时,BOPA配体的使用是获得高选择性的关键。此外,该反应机理涉及烷基自由基的参与。撰稿人:杉杉









目前评论: