近日,南京大学史壮志教授课题组在Sci. Adv.发表论文,报道了第一个涉及P(III)-导向C-H官能团化反应与外部氧化剂兼容的体系。其中,吲哚与一氧化碳和醇可以有效地进行C-H酯化反应,同时基于P(III)-导向基团的选择以及利用钯催化剂和苯醌作为外部氧化剂,从而实现高反应性和C7-选择性。此外,该反应使用廉价的羰基源,同时导向基团易于合成和除去,并且具有广泛的底物范围以及出色的位点选择性等特点。文章链接DOI:10.1126/sciadv.abd1378
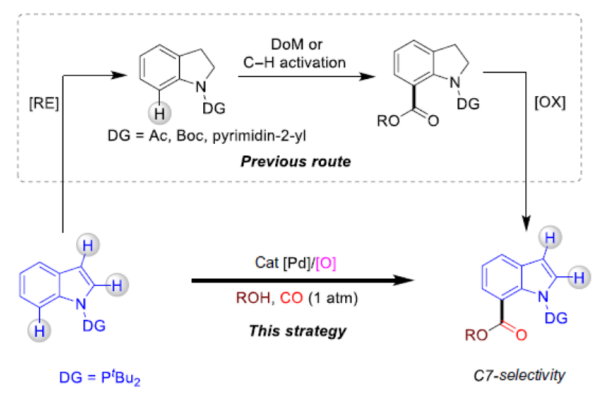
(图片来源:Sci. Adv.)
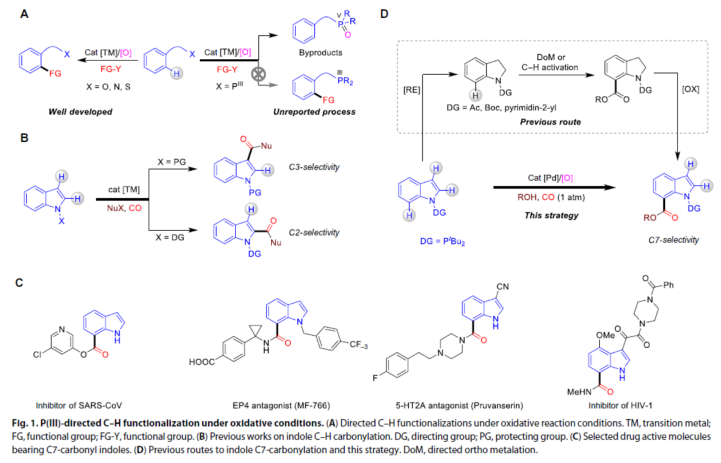
C-H键的功能化作为一种理想的合成途径,一直备受关注。由于复杂有机分子通常包含多个C-H键,并且活化能障差异很小,因此区域选择性的控制极具挑战。解决此类问题的有效策略是使用带有导向基团的底物,通过环金属化过程将金属传送到近端的C-H键。为了再生过渡金属催化剂,许多C-H官能团化反应需要外部的氧化剂。已开发出关于过渡金属与官能团中O,N或S原子的配位,这些均与氧化剂相容(Fig. 1A, left)。最近,也报道了在过渡金属催化下P(III)-螯合辅助的C-H功能化反应,但此类反应不能使用外部氧化剂。由于P(III)官能团通常在氧化剂存在下不稳定,易氧化成P(V)化合物,从而限制了该化学方法的适用性(Fig. 1A, right)。因此,与氧化剂兼容体系的开发,对于实现由P(III)-导向C-H功能化反应至关重要。在过渡金属催化杂环的C-H羰基化反应中,已充分利用一氧化碳作为廉价且丰富的C1源。通常,N-保护吲哚的C-H羰基化可以选择性地生成C3-羰基化吲哚(Fig. 1B, top)。最近,一些课题组报道了通过CO的插入,并将导向基团引入到N原子上,从而实现吲哚C2-位的C-H羰基化反应(Fig. 1B, bottom)。由于C2-和C3-固有的反应性,因此C7-位的选择性面临重大挑战。含有C7-羰基的吲哚对于药物的发现极为重要,同时具有多种药理活性,如SARS-CoV抑制剂、EP4拮抗剂、5-HT2A拮抗剂和HIV-抑制剂(Fig. 1C)。在这种情况下,一种间接获得这些化合物的方法包括将吲哚还原为二氢吲哚,然后进行邻位选择性酯化,然后进行氧化(Fig. 1D, top)。在此,南京大学史壮志教授课题组报道了以CO和醇作为羰基源,在钯催化下实现P(III)-导向的吲哚C7-选择性C-H酯化反应(Fig.1D, bottom)。作为反应的关键之处在于,寻找一种合适的氧化体系,不仅能够再生催化剂,同时还能够抑制P(III)化合物的氧化。
(图片来源:Sci. Adv.)
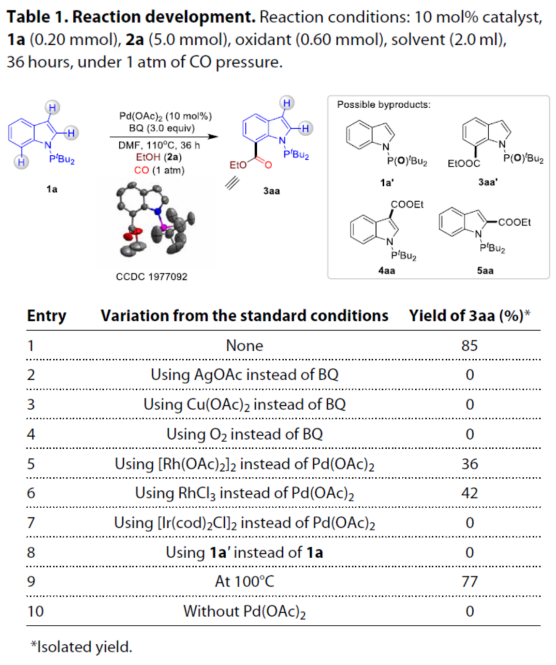
首先,作者以N-PtBu2吲哚1a、EtOH(2a)和CO气体作为模型底物,进行了三组分反应条件的筛选(Table 1)。当以10 mol%的Pd(OAc)2作为催化剂,3.0当量的苯醌(BQ)作为外部氧化剂,可在DMF溶剂中于110 ℃下反应,即可获得85%收率的C7-酯化产物3aa。
(图片来源:Sci. Adv.)
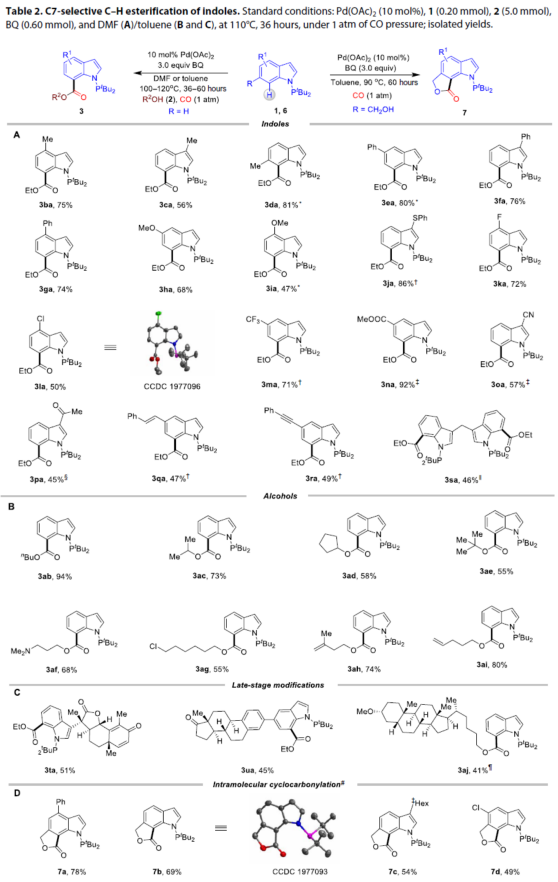
在获得上述最佳反应条件之后,作者对吲哚和醇的底物范围进行了扩展(Table 2)。首先,在对吲哚底物扩展时发现(Table 2A),在C3-至C6-位含有甲基、苯基、甲氧基、苯硫基、卤素、-CF3、酯、氰基、乙酰基等取代基时,均可顺利反应,获得相应的产物3ba-3pa。同时,烯基(3qa)和炔基(3ra)取代基的底物,也与体系兼容。并且,具有两个N-PtBu2基团的3,3'-二吲哚基甲烷1s可进行双C-H酯化反应,以中等的收率获得双吲哚产物3sa。其次,在对醇的底物扩展时发现(Table 2B),伯、仲和叔醇以及带有-NMe2、-Cl和烯基的伯醇,均与体系兼容,获得相应的产物3ab-3ai。同时,对于复杂的吲哚化合物与乙醇(2a)的后期酯化反应也很容易地进行,获得产物3ta-3ja,同时未产生任何外消旋作用(Table 2C)。值得注意的是,尽管在当前的反应条件下应使用大量或过量的醇,但未反应的醇可回收。此外,该策略还可用于分子内的环羰基化以实现内酯骨架的构建,如产物7a-7d(Table 2D)。
(图片来源:Sci. Adv.)
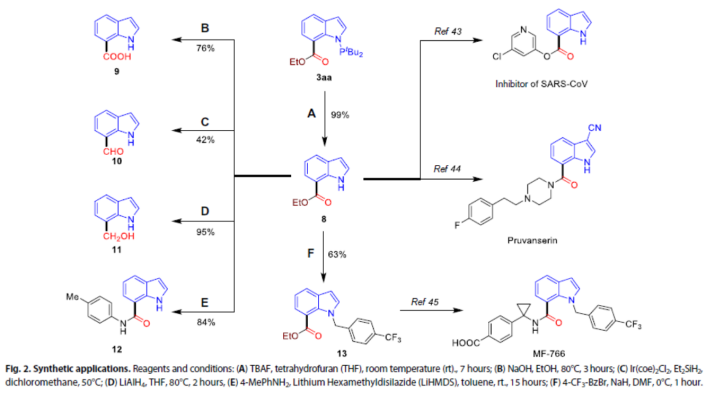
为了进一步证明反应的实用性,作者对产物进行了后期的衍生化(Fig. 2)。首先,在温和的条件下,使用氟化四丁基铵(TBAF)处理,可将产物3aa中N-PtBu2基团进行脱保护,获得易于进行各种转化的吲哚产物8,如经水解形成羧酸9,选择性还原形成醛10、醇11以及酰胺化为产物12。同时,8的苯甲酰化以63%的收率获得产物13,作为治疗炎症性疼痛候选药物MF-766的关键中间体。此外,还可以由吲哚8合成包括SARS-CoV抑制剂和5-HT2A受体拮抗剂Pruvanserin在内的生物学和药理活性分子。
(图片来源:Sci. Adv.)
最后,作者提出了一种可能的反应机理(Fig. 6)。首先,钯物种A螯合至吲哚1/6中,生成配合物B,再通过C的羧酸盐辅助C-H活化,从而产生钯环中间体D。随后,CO插入C-Pd键中生成配合物E。配合物E中的乙酸酯基团和醇2之间进行配体交换,经还原消除,可生成产物3和Pd(0)物种G。最后,BQ氧化G并原位形成AcOH可以重整催化物种A。此外,在吲哚4的情况下,配合物B的C-H金属化可生成单金属配合物I。该中间体经CO插入形成中间体II,再通过还原消除生成环化产物7以及Pd(0)物种G。

(图片来源:Sci. Adv.)
总结:南京大学史壮志教授课题组报道了一种Pd催化吲哚(含有N-PtBu2导向基团)C7-位定向位点选择性C-H酯化反应,并与外部氧化剂相容的体系。该策略有效地克服了传统上吲哚骨架中吡咯环的选择性。同时,选择BQ作为外部氧化剂可以防止导向基团的氧化。这种化学方法代表了P(III)-导向的C-H功能化实施的重要进展。








目前评论: