- A+
分享一篇发表在JACS上的文章,题目为Reversible Optical Control of Receptor Tyrosine Kinase Activity and ERK Dynamics Using Azobenzene-Carrying DNA Aptamer Agonist。文章的通讯作者为东京大学的Shinsuke Sando教授,其主要研究方向为功能性核酸/多肽和生物成像技术。

受体酪氨酸激酶(RTKs)是调节细胞功能的重要膜蛋白。一般地,RTK与其配体(通常为多肽,例如EGF)结合后发生二聚化,二聚化的RTK随后被磷酸化,并进一步激活下游信号分子。目前,在时间尺度上控制RTKs的活性主要依赖光遗传学技术,但该技术需要额外的基因工程改造。最近也报道了一些基于多肽或核酸适配体的RTKs激动剂,且通过在适配体上引入光反应性基团,可赋予其光响应性。但目前的光响应RTKs激动剂都涉及连接子的光切割,因此对它们的控制是不可逆的。在本文中,作者尝试开发一种基于DNA适配体的RTKs激动剂,它们能够在光作用下在活性和非活性结构之间可逆切换,从而实现对RTK的脉冲激活。
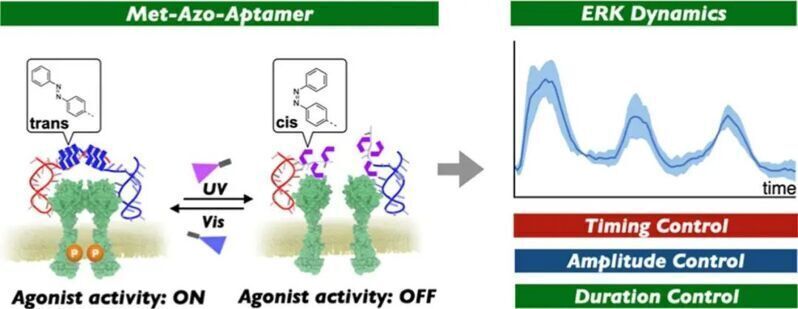
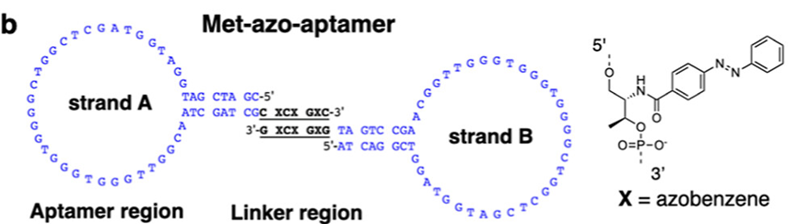
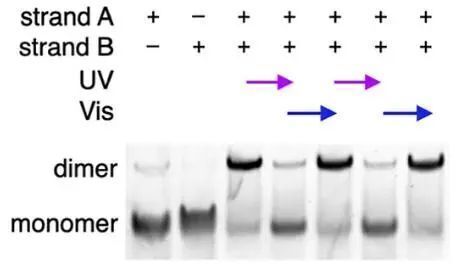
作者想利用一种经典的光响应分子偶氮苯实现他们的目的,该分子在蓝光和UV照射下发生顺反异构化。当被掺入DNA中时,只有反式构型的偶氮苯才能通过π-π堆叠作用稳定DNA双链。作者选择了c-Met 受体作为一种代表性的RTK进行后续研究。目前已有靶向c-Met 受体的核酸适配体,当适配体以单体形式与c-Met 受体作用时发挥抑制作用,而当两分子核酸适配体通过连接子相连时,则可诱导c-Met的二聚化激活。此处,作者通过向靶向c-Met 受体的适配体中引入含偶氮苯的非天然磷酸酯(X),构建了光控DNA基序。作者通过电泳证实了含该基序的适配体Met-Azo可在蓝光/UV的交替照射下实现连续的二聚化和解聚,也在体外证实了受光控二聚的Met-Azo具有c-Met激动活性。
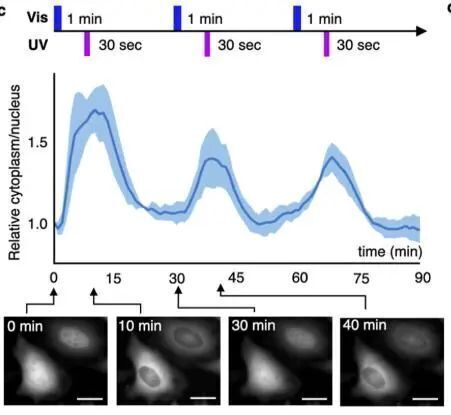
随后,作者使用Met-Azo适配体处理表达了激酶易位报告子(KTR)的HeLa细胞中,其表达的KTR可在c-Met 受体的下游ERK被磷酸化时从细胞核转移到细胞质。结果表明,在可见光/紫外交替照射下,KTR表现出了反复的易位行为,表明对ERK磷酸化水平的可逆控制。最后,作者也研究了这种脉冲信号对ERK激活动力学的影响,并成功实现了激活时刻、幅度和持续时间的人工调节。
总而言之,本文作者通过偶氮苯修饰的核酸适配体,实现了ERK信号通路的光控可逆激活。
本文作者:TYC
责任编辑:MB
DOI:10.1021/jacs.5c01559
原文链接:https://doi.org/10.1021/jacs.5c01559


目前评论: